Plasma-Proteine sind die stillen Architekten unserer Gesundheit, Milliarden winziger Moleküle, die unermüdlich in unserem Blutkreislauf zirkulieren und entscheidende Rollen bei allem spielen, von der Immunabwehr bis zum Stoffwechsel. Doch trotz ihrer allgegenwärtigen Präsenz und ihrer Bedeutung ist unser Verständnis darüber, was ihre Konzentrationen in unserem Blut antreibt und wie wir sie klinisch nutzen können, noch begrenzt. Eine bahnbrechende Studie, die modernste maschinelle Lernverfahren einsetzt, beleuchtet nun systematisch die Faktoren, die die Variation der Plasma-Proteinspiegel beeinflussen, und ebnet den Weg für eine neue Ära der Biomarker-Entdeckung und gezielten Therapie.
Diese Forschung analysierte nahezu 3.000 Proteinziele bei über 43.000 Individuen und identifizierte durchschnittlich 20 Faktoren, die bis zu 100% der Varianz in den Plasma-Proteinspiegeln erklären können. Die Ergebnisse zeigen, dass modifizierbare Merkmale – wie Lebensstil und Umweltfaktoren – einen größeren Einfluss haben als genetische Variationen, was wichtige Implikationen für die Präventivmedizin hat. Das Verständnis dieser komplexen Zusammenhänge ist fundamental, um die volle Leistungsfähigkeit der Proteomik für die Gesundheit des Menschen zu erschließen. Wie wir das Leben und die Bildung verstehen, so müssen wir auch die komplexen biologischen Prozesse erfassen, die unseren Körper steuern. indicatif bildung
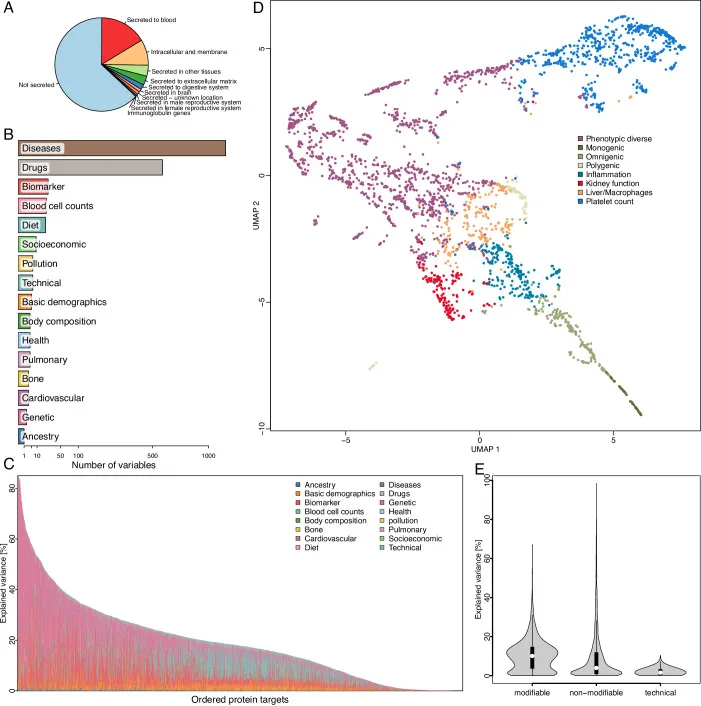 Koordinatensystem der Plasma-Protein-Variation
Koordinatensystem der Plasma-Protein-Variation
Das komplexe Geflecht der Protein-Variationen
Die Studie hat gezeigt, dass die Plasma-Proteine in verschiedene Cluster unterteilt werden können, basierend auf den erklärenden Faktoren ihrer Variation. Dies deutet darauf hin, dass bestimmte Proteingruppen ähnliche regulatorische Mechanismen oder gemeinsame Ursprünge haben könnten. Die identifizierten Faktoren, die die Proteinspiegel beeinflussen, reichen von demografischen Merkmalen über Lebensstilfaktoren bis hin zu genetischen Prädispositionen. Interessanterweise bleiben diese Faktoren weitgehend konsistent über verschiedene Geschlechter und ethnische Gruppen hinweg, was die Robustheit der Ergebnisse unterstreicht.
Ein zentraler Befund ist, dass modifizierbare Eigenschaften wie Ernährung, Bewegung oder chronische Erkrankungen im Durchschnitt 10,0 % der Varianz erklären, während genetische Variationen lediglich 3,9 % ausmachen. Dies eröffnet neue Perspektiven für Interventionen und präventive Maßnahmen, da viele dieser modifizierbaren Faktoren potenziell beeinflussbar sind. Dies kann als ein tiefgreifendes Verständnis dessen betrachtet werden, was es bedeutet, das volle Potenzial der menschlichen Gesundheit zu erreichen. etre bildung
Proteine als Brücke zwischen Zelltypen und Krankheiten
Die Forscher haben zudem einen Wissensgraphen etabliert, der die neuen Erkenntnisse mit genetischen Studien und Medikamentencharakteristika integriert. Dieser Graph ist ein mächtiges Werkzeug, um potenzielle Biomarker für Medikamenten-Zielengagements zu identifizieren. So können beispielsweise bestimmte Plasma-Proteine als “Marker-Gene” für spezifische Zelltypen dienen und Aufschluss darüber geben, wie diese Zelltypen mit Gesundheits- und Krankheitsindikatoren verknüpft sind.
Ein beeindruckendes Beispiel aus der Studie ist die Identifizierung der Matrix-Metalloproteinase 12 (MMP12) als krankheitsspezifischer Biomarker für das Bauchaortenaneurysma. Durch die Verknüpfung von Proteinspiegeln mit Krankheitsinzidenzdaten aus der UK Biobank konnten Assoziationen identifiziert werden, die auch nach Berücksichtigung anderer erklärender Faktoren bestehen blieben. Dies unterstreicht das enorme Potenzial von Plasma-Proteinen, nicht nur Risikofaktoren zu erkennen, sondern auch den Krankheitsverlauf zu verfolgen und die Wirksamkeit von Behandlungen zu überwachen.
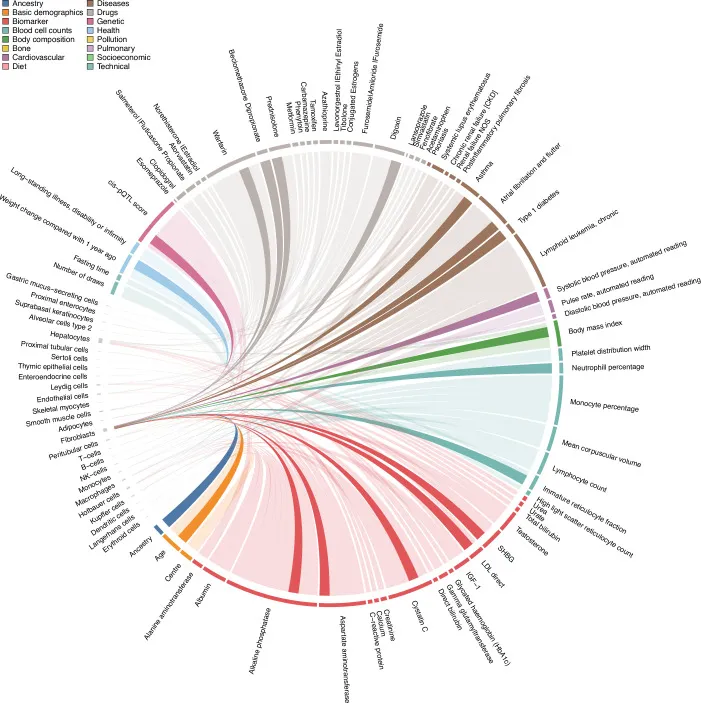 Plasma-Proteine verbinden Zelltypen mit Gesundheits- und Krankheitsindikatoren
Plasma-Proteine verbinden Zelltypen mit Gesundheits- und Krankheitsindikatoren
Stratifizierte Analyse: Geschlecht und Abstammung
Die Studie berücksichtigte auch geschlechts- und abstammungsstratifizierte Analysen, um mögliche Unterschiede in den erklärenden Faktoren zu untersuchen. Obwohl die Faktoren im Großen und Ganzen konsistent waren, wurden auch Nuancen festgestellt, die auf spezifische biologische Unterschiede hinweisen können. Diese detaillierten Analysen sind entscheidend, um die Präzisionsmedizin voranzutreiben und sicherzustellen, dass Biomarker und Therapien für alle Bevölkerungsgruppen gleichermaßen wirksam sind. Die Berücksichtigung dieser feinen Unterschiede ist ein zentraler Aspekt der modernen medizinischen Forschung.
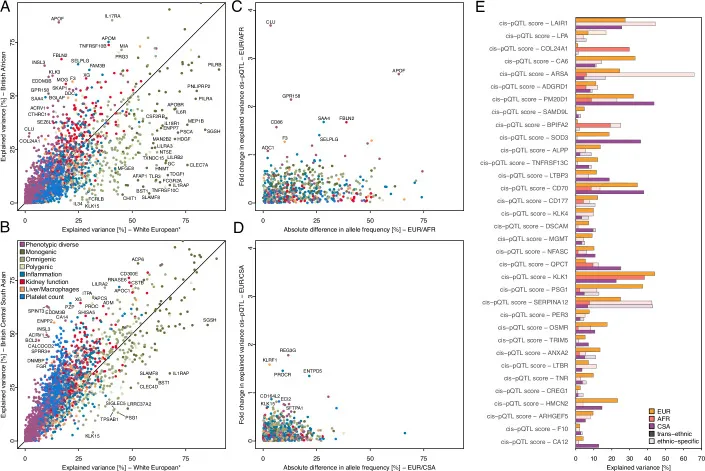 Zusammenfassung der abstammungsstratifizierten Analyse
Zusammenfassung der abstammungsstratifizierten Analyse
Die Ergebnisse zeigen, dass einige Proteine deutliche Unterschiede in der erklärten Varianz zwischen verschiedenen Abstammungsgruppen aufwiesen, was auf unterschiedliche genetische oder umweltbedingte Einflüsse hindeutet. Solche Erkenntnisse sind unerlässlich, um gesundheitliche Ungleichheiten besser zu verstehen und gezielte Interventionen zu entwickeln.
Die Bedeutung für die Krankheitserkennung und Medikamentenentwicklung
Ein wesentliches Ziel der Proteomik ist die Entdeckung von Biomarkern, die mit dem Einsetzen von Krankheiten assoziiert sind. Die Studie untersuchte Assoziationen zwischen Plasma-Proteinspiegeln und über 400 Krankheiten in der UK Biobank. Es wurden zahlreiche signifikante Assoziationen gefunden, von denen viele auch nach umfassender Adjustierung für erklärende Faktoren bestehen blieben. Dies bestätigt, dass diese Proteine nicht nur Korrelate, sondern möglicherweise kausale Faktoren oder wichtige Indikatoren für den Krankheitsbeginn sind.
Darüber hinaus bietet der entwickelte Wissensgraph eine einzigartige Ressource, um die Beziehungen zwischen Genen, Proteinen, Medikamenten und Krankheiten zu entschlüsseln. Dies kann die Identifizierung neuer Medikamenten-Ziele beschleunigen und die Entwicklung von Medikamenten erleichtern, die spezifisch auf bestimmte Proteinwege abzielen. Das Potenzial für die Entwicklung personalisierter Medikamente, die auf individuellen Proteinprofilen basieren, ist enorm.
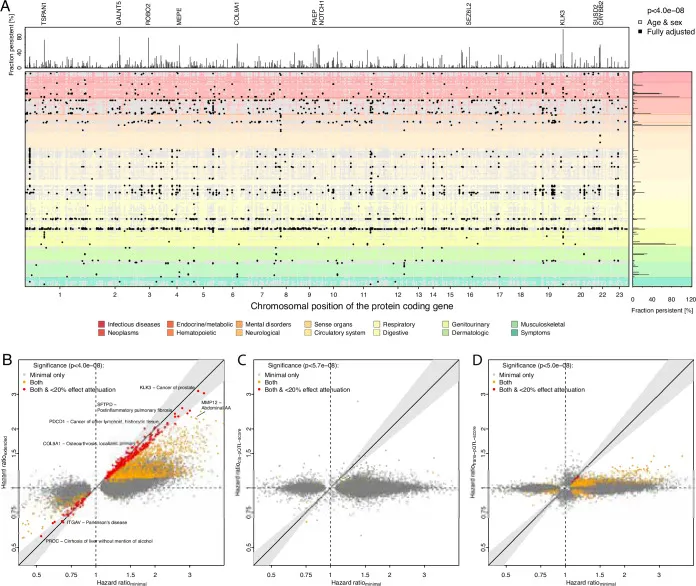 Protein-Inzidenz-Krankheits-Assoziationen
Protein-Inzidenz-Krankheits-Assoziationen
Phänotyp-Anreicherung und ein umfassendes Framework
Die Forscher haben auch ein breit anwendbares Framework zur Phänotyp-Anreicherung entwickelt, das als R-Paket (r-prodente) öffentlich verfügbar ist. Dieses Tool ermöglicht es anderen Wissenschaftlern, ihre eigenen Proteomik-Signaturen zu analysieren und mit einer breiten Palette von Phänotypen zu verknüpfen. Dies ist ein entscheidender Schritt zur Demokratisierung der Proteomik-Forschung und zur Beschleunigung der Entdeckung neuer Biomarker.
Beispiele für die Anwendung dieses Frameworks sind die Anreicherung von Proteomik-Signaturen, die sich nach einem Tag vollständiger Kalorienrestriktion unterscheiden, oder die Differenzierung zwischen gesunden Frauen und Frauen mit Eierstockkrebs. Solche Anwendungen demonstrieren die Vielseitigkeit und den praktischen Nutzen des entwickelten Tools. Die Bildung in diesem Bereich ist entscheidend, um zukünftige Entdeckungen zu ermöglichen. conditionnel passe bildung
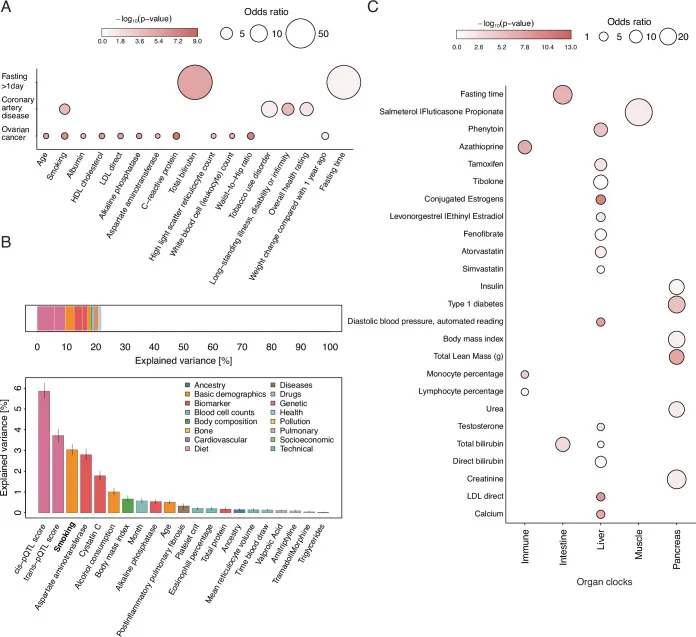 Phänotyp-Anreicherung von Plasma-Proteomik-Signaturen
Phänotyp-Anreicherung von Plasma-Proteomik-Signaturen
Ein integrierter Wissensgraph für die Zukunft der Medizin
Der integrierte Wissensgraph, der in dieser Studie vorgestellt wird, verbindet Einzelnukleotid-Polymorphismen (SNPs) mit Proteinen und Krankheiten und integriert Medikamentendaten. Dieser Graph ist eine dynamische und interaktive Ressource, die es ermöglicht, komplexe Beziehungen aufzudecken und Hypothesen für weitere Forschungen zu generieren. Die interaktive Web-Anwendung (omicscience.org/apps/prot_foundation) macht diese Erkenntnisse für die gesamte wissenschaftliche Gemeinschaft zugänglich.
Die Möglichkeiten, die sich aus diesem integrierten Ansatz ergeben, sind immens. Forscher können nun gezielt nach Proteinen suchen, die sowohl mit Krankheiten als auch mit bekannten Medikamenten-Zielen assoziiert sind, um so potenziell neue therapeutische Strategien zu identifizieren oder bestehende Medikamente neu zu positionieren. Dies ist ein Sprung nach vorne in unserem Bestreben, Krankheiten besser zu verstehen und wirksamere Behandlungen zu entwickeln.
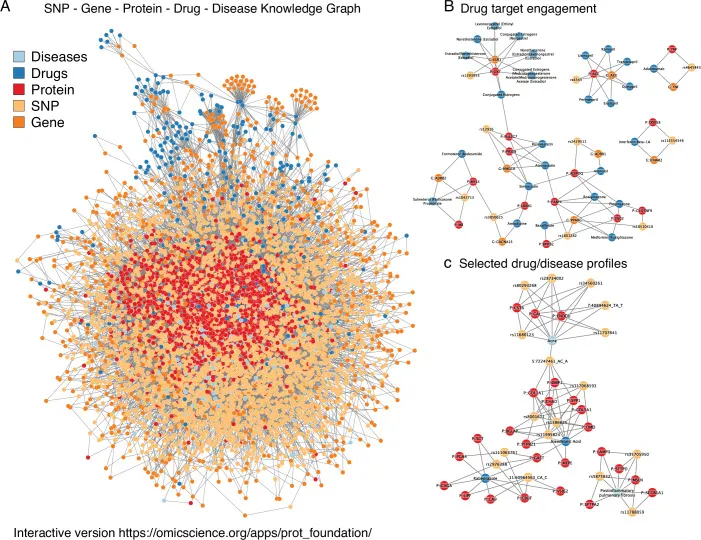 Integrierter Wissensgraph von Gen-, Protein-, Medikamenten- und Krankheitsbeziehungen
Integrierter Wissensgraph von Gen-, Protein-, Medikamenten- und Krankheitsbeziehungen
Fazit
Die detaillierte Untersuchung der Faktoren, die die Plasma-Proteinspiegel beeinflussen, und die Entwicklung eines umfassenden Wissensgraphen stellen einen Meilenstein in der Proteomik-Forschung dar. Diese Erkenntnisse verbessern nicht nur unser grundlegendes Verständnis der menschlichen Biologie, sondern bieten auch praktische Werkzeuge für die Identifizierung robuster Biomarker, die Entwicklung gezielter Therapien und die Beschleunigung der medizinischen Forschung. Durch die systematische Entschlüsselung der Sprache der Plasma-Proteine rücken wir einem personalisierten und präventiven Gesundheitswesen einen großen Schritt näher. Entdecken Sie die Möglichkeiten, die diese Forschung für die Zukunft der Medizin eröffnet, und bleiben Sie auf dem Laufenden über die neuesten Entwicklungen auf Shock Naue!
Referenzen
- The Author(s). (2025). Proteomic techniques now measure thousands of proteins circulating in blood at population scale… [Abstract und begleitende Daten aus der Originalpublikation].
